ગેલ્વેનિક કોષો અને બેટરીઓ - ઉપકરણ, કામગીરીના સિદ્ધાંત, પ્રકારો
વિદ્યુત ઊર્જાના ઓછા પાવર સ્ત્રોતો
ગેલ્વેનિક કોષો અને બેટરીનો ઉપયોગ પોર્ટેબલ ઇલેક્ટ્રિકલ અને રેડિયો સાધનોને પાવર કરવા માટે થાય છે.
ગેલ્વેનિક કોષો - આ એક સમયની ક્રિયાઓના સ્ત્રોત છે, સંચયકો - ફરીથી વાપરી શકાય તેવા ક્રિયા સ્ત્રોતો.

સૌથી સરળ ગેલ્વેનિક તત્વ
સૌથી સરળ તત્વ બે સ્ટ્રીપ્સમાંથી બનાવી શકાય છે: તાંબુ અને જસત પાણીમાં ડૂબીને સલ્ફ્યુરિક એસિડથી સહેજ એસિડિફાઇડ. જો ઝીંક એટલુ શુદ્ધ હોય કે કોઈ સ્થાનિક પ્રતિક્રિયાઓ ન થાય, તો જ્યાં સુધી તાંબુ અને જસત એકસાથે લાવવામાં ન આવે ત્યાં સુધી કોઈ નોંધપાત્ર ફેરફાર થશે નહીં.
જો કે, સ્ટ્રીપ્સમાં અલગ સંભવિત હોય છે, એક બીજાના સંદર્ભમાં, અને જ્યારે વાયર દ્વારા જોડાયેલ હોય, ત્યારે દેખાશે. વીજળી… આ ક્રિયા દ્વારા જસતની પટ્ટી ધીમે ધીમે ઓગળી જશે અને કોપર ઇલેક્ટ્રોડની નજીક ગેસના પરપોટા બનશે, તેની સપાટી પર એકત્ર થશે. આ ગેસ ઇલેક્ટ્રોલાઇટ દ્વારા ઉત્પન્ન થયેલ હાઇડ્રોજન છે. વાયરની સાથે કોપર સ્ટ્રીપમાંથી ઝીંક સ્ટ્રીપમાં વિદ્યુત પ્રવાહ વહે છે અને તેમાંથી ઈલેક્ટ્રોલાઈટ દ્વારા પાછા કોપર તરફ જાય છે.
ધીમે ધીમે, ઇલેક્ટ્રોલાઇટના સલ્ફ્યુરિક એસિડને ઝીંક ઇલેક્ટ્રોડના ઓગળેલા ભાગમાંથી બનેલા ઝીંક સલ્ફેટ દ્વારા બદલવામાં આવે છે. આ સેલનું વોલ્ટેજ ઘટાડે છે. જો કે, તાંબા પર ગેસના પરપોટાની રચનાને કારણે વોલ્ટેજમાં પણ વધુ ઘટાડો થાય છે. બંને ક્રિયાઓ 'ધ્રુવીકરણ'નું કારણ બને છે. આવી વસ્તુઓનું લગભગ કોઈ વ્યવહારુ મૂલ્ય નથી.
ગેલ્વેનિક કોષોના મહત્વપૂર્ણ પરિમાણો
ગેલ્વેનિક કોષો દ્વારા આપવામાં આવતા વોલ્ટેજની તીવ્રતા ફક્ત તેમના પ્રકાર અને ઉપકરણ પર આધારિત છે, એટલે કે, ઇલેક્ટ્રોડ્સની સામગ્રી અને ઇલેક્ટ્રોલાઇટની રાસાયણિક રચના પર, પરંતુ તે કોષોના આકાર અને કદ પર આધારિત નથી.
ગેલ્વેનિક કોષ જે પ્રવાહ પ્રદાન કરી શકે છે તે તેના આંતરિક પ્રતિકાર દ્વારા મર્યાદિત છે.
ગેલ્વેનિક સેલની ખૂબ જ મહત્વપૂર્ણ લાક્ષણિકતા છે વિદ્યુત ક્ષમતા… વિદ્યુત ક્ષમતા એટલે કે ગેલ્વેનિક અથવા સ્ટોરેજ સેલ તેની સમગ્ર કામગીરી દરમિયાન, એટલે કે અંતિમ વિસર્જનની શરૂઆત સુધી વિતરિત કરવામાં સક્ષમ હોય તે વીજળીનો જથ્થો.
કોષ દ્વારા આપવામાં આવેલી ક્ષમતા એમ્પીયરમાં દર્શાવવામાં આવેલા ડિસ્ચાર્જ કરંટની મજબૂતાઈના ગુણાકાર દ્વારા નક્કી કરવામાં આવે છે, જે દરમિયાન સેલ પૂર્ણ ડિસ્ચાર્જની શરૂઆત સુધી ડિસ્ચાર્જ કરવામાં આવ્યો હતો. તેથી, ક્ષમતા હંમેશા એમ્પીયર-કલાકો (Ah) માં દર્શાવવામાં આવે છે.

સેલની ક્ષમતાના મૂલ્ય દ્વારા, તે અગાઉથી નક્કી કરવું પણ શક્ય છે કે તે સંપૂર્ણ ડિસ્ચાર્જની શરૂઆત પહેલાં કેટલા કલાક કામ કરશે. આ કરવા માટે, તમારે આ તત્વ માટે માન્ય ડિસ્ચાર્જ વર્તમાનની શક્તિ દ્વારા ક્ષમતાને વિભાજીત કરવાની જરૂર છે.
જો કે, ક્ષમતા સખત રીતે સ્થિર નથી. તે તત્વની ઓપરેટિંગ શરતો (મોડ) અને અંતિમ ડિસ્ચાર્જ વોલ્ટેજના આધારે એકદમ મોટી મર્યાદામાં બદલાય છે.
જો સેલ મહત્તમ વર્તમાન પર વિસર્જિત થાય છે અને વધુમાં, વિક્ષેપો વિના, તે ઘણી ઓછી ક્ષમતા આપશે. તેનાથી વિપરિત, જ્યારે સમાન કોષને નીચા પ્રવાહ પર અને વારંવાર અને પ્રમાણમાં લાંબા વિક્ષેપો સાથે વિસર્જિત કરવામાં આવે છે, ત્યારે કોષ તેની સંપૂર્ણ ક્ષમતા છોડી દેશે.
કોષની ક્ષમતા પર અંતિમ ડિસ્ચાર્જ વોલ્ટેજના પ્રભાવ માટે, તે ધ્યાનમાં રાખવું જોઈએ કે ગેલ્વેનિક સેલના ડિસ્ચાર્જ દરમિયાન, તેનું ઓપરેટિંગ વોલ્ટેજ સમાન સ્તરે રહેતું નથી, પરંતુ ધીમે ધીમે ઘટતું જાય છે.
ઇલેક્ટ્રોકેમિકલ કોષોના સામાન્ય પ્રકારો
સૌથી સામાન્ય ગેલ્વેનિક કોષો મેંગેનીઝ-ઝીંક, મેંગેનીઝ-એર, એર-ઝીંક અને મીઠું અને આલ્કલાઇન ઇલેક્ટ્રોલાઇટ્સ સાથે પારા-ઝીંક પ્રણાલીઓ છે. મીઠું ઇલેક્ટ્રોલાઇટ સાથેના સુકા મેંગેનીઝ-ઝીંક કોષોમાં પ્રારંભિક વોલ્ટેજ 1.4 થી 1.55 V હોય છે, ઓપરેશનની અવધિ સવારે 7 થી 340 સુધી -20 થી -60 ના આસપાસના તાપમાને
આલ્કલાઇન ઇલેક્ટ્રોલાઇટ સાથે સુકા ઝીંક-મેંગેનીઝ અને ઝીંક-એર કોષો 0.75 થી 0.9 V નો વોલ્ટેજ ધરાવે છે અને 6 કલાકથી 45 કલાકનો કાર્યકારી સમય ધરાવે છે.
શુષ્ક પારો-ઝીંક કોષોમાં 1.22 થી 1.25 V નો પ્રારંભિક વોલ્ટેજ અને 24 કલાકથી 55 કલાકનો કાર્યકારી સમય હોય છે.
શુષ્ક પારો-ઝીંક કોષો 30 મહિના સુધીની સૌથી લાંબી બાંયધરીકૃત શેલ્ફ લાઇફ ધરાવે છે.

બેટરીઓ
બેટરીઓ આ ગૌણ ઇલેક્ટ્રોકેમિકલ કોષો છે. ગેલ્વેનિક કોષોથી વિપરીત, એસેમ્બલી પછી તરત જ બેટરીમાં કોઈ રાસાયણિક પ્રક્રિયા થતી નથી.
બેટરીને વિદ્યુત ચાર્જની હિલચાલ સાથે સંકળાયેલ રાસાયણિક પ્રતિક્રિયાઓ શરૂ કરવા માટે, તેના ઇલેક્ટ્રોડ્સ (અને અંશતઃ ઇલેક્ટ્રોલાઇટની) ની રાસાયણિક રચનાને યોગ્ય રીતે બદલવી જરૂરી છે.ઇલેક્ટ્રોડ્સની રાસાયણિક રચનામાં આ ફેરફાર બેટરીમાંથી પસાર થતા ઇલેક્ટ્રિક પ્રવાહની ક્રિયા હેઠળ થાય છે.
તેથી, બેટરીને વિદ્યુતપ્રવાહ ઉત્પન્ન કરવા માટે, તે પહેલા અમુક બાહ્ય વર્તમાન સ્ત્રોતમાંથી સીધા વિદ્યુત પ્રવાહથી "ચાર્જ" થવી જોઈએ.
બેટરીઓ પરંપરાગત ગેલ્વેનિક કોષોથી એ હકીકતમાં પણ અલગ પડે છે કે, ડિસ્ચાર્જ પછી, તેઓ રિચાર્જ કરી શકાય છે. સારી સંભાળ સાથે અને સામાન્ય ઓપરેટિંગ પરિસ્થિતિઓમાં, બેટરી હજારો ચાર્જ અને ડિસ્ચાર્જ સુધી ટકી શકે છે. બેટરી સંચાલિત ઉપકરણ
બેટરી સંચાલિત ઉપકરણ
હાલમાં, સીસા અને કેડમિયમ-નિકલ બેટરીનો વ્યવહારમાં મોટાભાગે ઉપયોગ થાય છે. સલ્ફ્યુરિક એસિડના પ્રથમ દ્રાવણમાં ઇલેક્ટ્રોલાઇટ તરીકે કામ કરે છે, અને પાણીમાં આલ્કલીના બીજા દ્રાવણમાં. લીડ-એસિડ બેટરીઓને એસિડ અને નિકલ-કેડમિયમ-આલ્કલાઇન બેટરી પણ કહેવામાં આવે છે.
બેટરીના સંચાલનનો સિદ્ધાંત ઇલેક્ટ્રોડ્સના ધ્રુવીકરણ પર આધારિત છે વિદ્યુત વિચ્છેદન-વિશ્લેષણ દરમિયાન... સૌથી સરળ એસિડ બેટરી નીચે પ્રમાણે રચાયેલ છે: તે ઇલેક્ટ્રોલાઇટમાં ડૂબેલી બે લીડ પ્લેટ છે. રાસાયણિક અવેજીની પ્રતિક્રિયાના પરિણામે, પ્લેટો લીડ સલ્ફેટ PbSO4 ના પાતળા આવરણથી ઢંકાયેલી હોય છે, જે Pb + H2SO4 = PbSO4 + H2 સૂત્રમાંથી નીચે મુજબ છે.
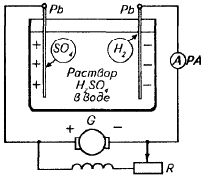
એસિડ બેટરી ઉપકરણ
પ્લેટોની આ સ્થિતિ વિસર્જિત બેટરીને અનુરૂપ છે. જો બેટરી હવે ચાર્જિંગ માટે ચાલુ છે, એટલે કે, સીધા વર્તમાન જનરેટર સાથે જોડાયેલ છે, તો વિદ્યુત વિચ્છેદન-વિશ્લેષણને કારણે તેમાં પ્લેટોનું ધ્રુવીકરણ શરૂ થશે. બેટરી ચાર્જ કરવાના પરિણામે, તેની પ્લેટો ધ્રુવીકૃત થાય છે, એટલે કે તેમની સપાટી પરના પદાર્થને અને સજાતીય (PbSO4) થી અલગ (Pb અને PbO2) માં બદલો.
બેટરી વર્તમાન સ્ત્રોત બની જાય છે, જેમાં સકારાત્મક ઇલેક્ટ્રોડ તરીકે લીડ ડાયોક્સાઇડ સાથે કોટેડ પ્લેટ અને નકારાત્મક ઇલેક્ટ્રોડ તરીકે સ્વચ્છ લીડ પ્લેટ હોય છે.
ચાર્જિંગના અંત સુધીમાં, તેમાં વધારાના સલ્ફ્યુરિક એસિડ પરમાણુઓના દેખાવને કારણે ઇલેક્ટ્રોલાઇટની સાંદ્રતા વધે છે.
આ લીડ-એસિડ બેટરીની લાક્ષણિકતાઓમાંની એક છે: તેનો ઇલેક્ટ્રોલાઇટ તટસ્થ રહેતો નથી અને પોતે બેટરીની કામગીરી દરમિયાન રાસાયણિક પ્રતિક્રિયાઓમાં ભાગ લે છે.
ડિસ્ચાર્જના અંત સુધીમાં, બેટરીની બંને પ્લેટો ફરીથી લીડ સલ્ફેટથી આવરી લેવામાં આવે છે, જેના પરિણામે બેટરી વર્તમાનનો સ્ત્રોત બનવાનું બંધ કરે છે. બેટરી ક્યારેય આ સ્થિતિમાં લાવવામાં આવતી નથી. પ્લેટો પર લીડ સલ્ફેટની રચનાને કારણે, સ્રાવના અંતે ઇલેક્ટ્રોલાઇટની સાંદ્રતા ઘટે છે. જો બેટરી ચાર્જ કરવામાં આવે છે, તો તેને ફરીથી ડિસ્ચાર્જ પર મૂકવા માટે ફરીથી ધ્રુવીકરણ થઈ શકે છે, વગેરે.
બેટરી કેવી રીતે ચાર્જ કરવી
બેટરી ચાર્જ કરવાની ઘણી રીતો છે. સૌથી સરળ બેટરીનું સામાન્ય ચાર્જિંગ છે, જે નીચે પ્રમાણે કરવામાં આવે છે. શરૂઆતમાં, 5-6 કલાક માટે, દરેક બેટરીનું વોલ્ટેજ 2.4 V સુધી ન પહોંચે ત્યાં સુધી ચાર્જિંગ ડબલ સામાન્ય પ્રવાહ પર કરવામાં આવે છે.
સામાન્ય ચાર્જિંગ વર્તમાન ફોર્મ્યુલા Aztax = Q/16 દ્વારા નક્કી કરવામાં આવે છે
જ્યાં ક્યૂ — બેટરીની નજીવી ક્ષમતા, આહ.
તે પછી, ચાર્જિંગ વર્તમાનને સામાન્ય મૂલ્યમાં ઘટાડવામાં આવે છે અને ચાર્જિંગ સમાપ્ત થવાના સંકેતો દેખાય ત્યાં સુધી 15-18 કલાક સુધી ચાર્જિંગ ચાલુ રહે છે.
આધુનિક બેટરીઓ
નિકલ-કેડમિયમ અથવા આલ્કલાઇન બેટરીઓ લીડ બેટરી કરતાં ઘણી પાછળથી દેખાઈ, અને તેની સરખામણીમાં રાસાયણિક પ્રવાહના વધુ આધુનિક સ્ત્રોતો છે.લીડ બેટરીઓ પર આલ્કલાઇન બેટરીનો મુખ્ય ફાયદો પ્લેટોના સક્રિય સમૂહના સંબંધમાં તેમના ઇલેક્ટ્રોલાઇટની રાસાયણિક તટસ્થતામાં રહેલો છે. તેથી, આલ્કલાઇન બેટરીનું સ્વ-ડિસ્ચાર્જ લીડ-એસિડ બેટરી કરતા નોંધપાત્ર રીતે ઓછું છે. આલ્કલાઇન બેટરીના સંચાલનનો સિદ્ધાંત પણ વિદ્યુત વિચ્છેદન-વિશ્લેષણ દરમિયાન ઇલેક્ટ્રોડ્સના ધ્રુવીકરણ પર આધારિત છે.
રેડિયો સાધનોને પાવર આપવા માટે, સીલબંધ કેડમિયમ-નિકલ બેટરીઓ બનાવવામાં આવે છે, જે -30 થી +50 OC તાપમાને અસરકારક હોય છે અને 400 - 600 ચાર્જ-ડિસ્ચાર્જ ચક્રનો સામનો કરે છે. આ સંચયકો કોમ્પેક્ટ પેરેલેલેપાઇપ્ડ અને ડિસ્કના રૂપમાં થોડા ગ્રામથી કિલોગ્રામ સુધીના વજનમાં બનાવવામાં આવે છે.
નિકલ-હાઈડ્રોજન બેટરી સ્વાયત્ત વસ્તુઓને શક્તિ આપવા માટે બનાવવામાં આવે છે. નિકલ-હાઈડ્રોજન બેટરીની ચોક્કસ ઉર્જા 50 — 60 Wh kg-1 છે.




